2024年11月8日,中山大学肿瘤防治中心麦海强教授团队开展的“新辅助及辅助特瑞普利单抗联合同期放化疗治疗高危局部区域晚期鼻咽癌的II期随机对照双盲研究”在国际顶级肿瘤学期刊《柳叶刀肿瘤学》(Lancet Oncology)在线发表。该研究首次发现在同期放化疗基础上增加特瑞普利单抗(PD-1抗体)新辅助和辅助治疗显著提高了高危局部晚期鼻咽癌患者生存率。

研究结果在《柳叶刀肿瘤》在线发表
鼻咽癌是我国比较高发的恶性肿瘤,每年的新发病例数占据全球病例的近一半(47%)。由于发病部位隐蔽而且症状不特异,约75%鼻咽癌患者初诊时疾病达到局部晚期。对于局部区域晚期患者,同期放化疗是局部区域晚期鼻咽癌的标准治疗方案。然而接受标准治疗后仍有20%-30%的患者会出现复发或转移,尤其是治疗前血浆EBV DNA高水平患者,疾病进展或复发的风险更高。因而,探索可增效、减毒的新策略来满足高危患者的治疗需求迫在眉睫。
鼻咽癌和EBV感染密切相关,肿瘤组织大量淋巴细胞浸润及PD-L1表达升高,也就是俗语说的“热肿瘤”,因此可能非常适合免疫治疗。当前,晚期鼻咽癌已进入免疫治疗时代,PD-1单抗联合化疗已成为复发/转移性鼻咽癌患者的标准一线治疗方案,而局部区域晚期鼻咽癌的选方案尚未确立。随着免疫治疗在晚期鼻咽癌患者中展现出持久疗效和良好耐受性,其在局晚期患者中的应用逐渐成为研究新趋势,并取得了一定的成果。
既往研究表明,在放疗前新辅助阶段加上PD-1单抗治疗可以在放疗前充分激活抗肿瘤免疫反应,活化的肿瘤特异性T细胞不仅可以杀伤原位肿瘤,还能通过机体迁移寻找并消灭远处微小转移灶。同时期放化疗后辅助阶段加用PD-1单抗治疗可以进一步强化免疫监视作用,清除鼻咽残留病灶及远处微小转移灶,进而减少复发转移、改善局晚期鼻咽癌患者的生存。同时,考虑到放疗阶段大体积的颈部淋巴结预防照射会直接消除记忆性淋巴细胞而削弱免疫治疗的疗效,以及辐射可能会改变肿瘤微环境从而减弱PD-1单抗的抗肿瘤免疫反应,所以本研究在同期放化疗阶段不联用PD-1抗体。通过血浆EBV DNA筛选出预后更差的局部区域晚期鼻咽癌患者,若在同期放化疗基础上增加PD-1单抗新辅助和辅助治疗,即“免疫三明治”治疗模式,有望进一步提高这部分高危患者的生存率。为了验证这一假设,麦海强教授团队发起了这项II期随机研究,以评估这一治疗方案的有效性和安全性。
该项随机、双盲、安慰剂对照的II期研究共纳入150名III期和IVa期且血浆高EBV DNA水平的高危局部区域晚期鼻咽癌患者,以2:1的比例随机接受特瑞普利单抗(240 mg,每两周一次)或安慰剂诱导治疗2周期后,接受同期放化疗,之后接受特瑞普利单抗(240 mg,每三周一次)或安慰剂维持治疗8周期。
研究结果显示,在中位随访37.8个月时,与单纯同期放化疗组相比,特瑞普利单抗联合治疗组的主要终点2年无进展生存率显著提高(92.0% vs. 74.0%),将疾病进展或死亡风险降低了60%。在次要终点上,相较于单纯同期放化疗组,特瑞普利单抗联合治疗组的3年总体生存率显著提高(99.0% vs. 90.0%)。此外,3年累积远处转移率从20.2%降低到9.6%,3年累积局部区域复发率从17.0%下降到3.7%。在安全性方面,特瑞普利单抗联合治疗组未发现新的安全性信号,两组≥3级治疗相关不良事件发生率相似(73.7% vs 68.0%)。
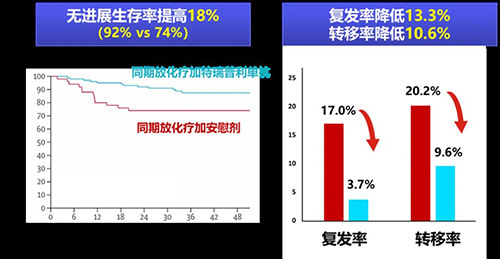
除了在无进展生存率及总体生存率上的显著改善,特瑞普利单抗新辅助治疗在患者 EBV-DNA 水平的清零上也展现了强大的作用,17.0%的受试者接受新辅助特瑞普利单抗治疗两个周期后,在同期放化疗前检测不到血浆EBV DNA,并且在事后分析中发现这部分患者3年无进展生存率达100%,这表明他们是免疫治疗的合适人群。
本次开展的II期研究是免疫治疗在高危局部区域晚期鼻咽癌中应用价值的一次探索,覆盖了新辅助治疗和后续的巩固治疗阶段。本研究证实了相较于单纯同期放化疗,在同期放化疗基础上联合特瑞普利单抗新辅助和辅助治疗,可以显著改善高危局部区域晚期鼻咽癌患者的生存率,降低疾病进展风险,同时具有可接受的安全性。这一“免疫三明治”模式或可成为局部区域晚期鼻咽癌的潜在治疗新方案,值得开展三期大样本研究以夯实该方案的临床获益。相信随着更多循证医学证据和临床实践经验的积累,局部区域晚期鼻咽癌的治疗模式将不断优化,从而改善患者的肿瘤局部区域控制,减少远处转移风险,延长生存。
中山大学肿瘤防治中心麦海强教授、陈秋燕教授、唐林泉副主任医师为该论文的共同通讯作者。中山大学肿瘤防治中心刘赛兰副主任医师、李晓韵医师、杨金昊博士、温冬香博士、郭姗姗副主任医师、刘丽婷副主任医师、李轶甫博士为该论文共同第一作者。(通讯员:文朝阳、陈鋆、郑敏珊)

麦海强团队成员合照
 39健康网
39健康网 恶性脂肪肉瘤症状2025-02-27
恶性脂肪肉瘤症状2025-02-27 上皮内淋巴浸润严重吗2025-02-27
上皮内淋巴浸润严重吗2025-02-27 子宫免疫组化结果怎么看2025-02-27
子宫免疫组化结果怎么看2025-02-27 腺瘤需要做手术吗2025-02-27
腺瘤需要做手术吗2025-02-27 活检结果低度鳞状上皮内病变2025-02-27
活检结果低度鳞状上皮内病变2025-02-27 上皮内瘤变的症状2025-02-27
上皮内瘤变的症状2025-02-27 钙化点是不是都是癌前兆2025-02-27
钙化点是不是都是癌前兆2025-02-27 肌上皮癌会不会传染2025-02-27
肌上皮癌会不会传染2025-02-27 盐城治疗肾结石权威医院推荐2025-02-27
盐城治疗肾结石权威医院推荐2025-02-27 马鞍山治皮肤过敏医院哪家专业2025-02-27
马鞍山治皮肤过敏医院哪家专业2025-02-27 乌海治早泄医院哪家比较权威2025-02-27
乌海治早泄医院哪家比较权威2025-02-27
 汕头哪家医院治咽炎好2025-02-27
汕头哪家医院治咽炎好2025-02-27 池州男性不育去哪里治比较好2025-02-27
池州男性不育去哪里治比较好2025-02-27 咸宁治疗青光眼权威医院推荐2025-02-27
咸宁治疗青光眼权威医院推荐2025-02-27
 自卑心理评估,测你内心真实的自卑程度心理测试
自卑心理评估,测你内心真实的自卑程度心理测试 子宫癌自测心理测试
子宫癌自测心理测试








