中肿徐瑞华教授发表研究成果,为EBV阳性胃癌患者提供了新的治疗方向
2023年9月21日,中山大学肿瘤防治中心徐瑞华教授团队在国际知名期刊Signal Transduction and Targeted Therapy发表了题为“动态单细胞图谱揭示EB病毒介导T细胞耗竭以及免疫治疗反应的关键细胞亚群”的研究成果。研究人员通过动态单细胞转录组测序和配对的免疫组库(scTCR/BCR-seq),对免疫联合化疗前后EB病毒阳性和阴性胃癌的肿瘤免疫微环境进行了精细的解析。该研究成果揭示了胃癌患者治疗敏感性的免疫学基础,发现了免疫治疗反应的关键性T细胞亚群,为EBV阳性胃癌患者提供了新的治疗方向。

胃癌是严重危害国民健康的恶性疾病,其发病率和死亡率均占恶性肿瘤前三位。免疫检查点抑制剂(ICIs)的使用为肿瘤治疗带来新的曙光,但在胃癌治疗中,ICIs单药的有效率只有10%左右,因此有必要探索疗效预测指标以甄别获益人群,避免无效用药。既往文献报道EB病毒阳性胃癌患者对PD-1抗体的有效率(约为25%)显著高于整体胃癌患者(10%)。EB病毒感染如何影响免疫疗效是亟待探究的重要科学问题。
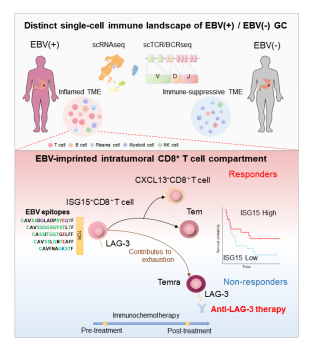
在该研究中,通过系统比较EB病毒阳性和阴性胃癌患者的肿瘤微环境免疫特征,研究人员发现EB病毒阳性胃癌微环境为免疫炎症型,具有丰富的T细胞和B细胞浸润,体现了EBV感染、免疫细胞生态系统和肿瘤之间复杂的相互作用。EB病毒阴性胃癌则呈现出“冷肿瘤”微环境,T细胞和B细胞浸润较少且免疫抑制性细胞(髓系细胞)浸润较多。
进一步分析发现,在EBV阳性胃癌患者中,存在EBV抗原特异性CD8+T细胞亚群(ISG-15+CD8+ T细胞),这群细胞为前体耗竭型T细胞,表现出干细胞性质:包括较强的增殖能力和分化为耗竭型T细胞的潜能。有意思的是,研究者发现ISG-15+CD8+ T细胞在其他EB病毒相关肿瘤(肝内胆管癌和鼻咽癌)亦普遍存在。研究人员通过动态精确对比不同免疫细胞的组成成分和比例变化与治疗效果的关联,发现更高基线水平的ISG-15+CD8+ T细胞能够预测更好的免疫治疗响应。I型干扰素的高反应性是EB病毒相关肿瘤浸润T细胞活化的特征之一。
此外,研究人员发现治疗有效的患者治疗后肿瘤微环境中高表达CXCL13的CD8+T细胞出现明显克隆扩增,显示出较强的肿瘤杀伤能力。而非响应患者肿瘤浸润CD8+T细胞则高表达抑制性免疫检查点-LAG3,并逐渐进入终末耗竭状态。因此,推测LAG-3可能是EB病毒阳性患者免疫治疗的潜在新靶点。基于这个发现,研究团队推荐了两位难治性EBV阳性胃癌患者参加LAG3抑制剂的临床试验,发现LAG3抗体有效抑制肿瘤生长并降低外周血EBV-DNA拷贝数。靶向LAG3可能是EB病毒阳性胃癌患者新的治疗方向。
研究机制示意图
中山大学肿瘤防治中心徐瑞华教授、澳门大学健康科学学院张海燕副研究员为该研究论文的共同通讯作者。中山大学肿瘤防治中心邱妙珍主任医师、王朝晔硕士研究生、伍芷莹博士、赵齐副研究员,南方医科大学赵志斌副研究员为该研究论文的共同第一作者。
论文链接:https://www.nature.com/articles/s41392-023-01622-1
(通讯员:陈鋆、郑敏珊、赵现廷)

