8月31日,奥希替尼获中国药监局(NMPA)批准用于一线治疗EGFR突变阳性晚期或转移性非小细胞肺癌(NSCLC)成人患者的消息刷爆了朋友圈,这一肺癌界的“传奇巨星”将继续照亮中国患者。
肺癌不仅是中国,也是全世界发病率和死亡率最高的恶性肿瘤。我国每年新发病的肺癌患者超过70万人,其中近三分之二的患者初诊时已失去手术机会。靶向治疗的出现对占肺癌近80%的非小细胞肺癌治疗取得较好效果也起了很大的推动作用。
在中国的非小细胞肺癌患者中,约有30%-40%发生EGFR突变,奥希替尼是第三代口服、不可逆的选择性EGFR突变抑制剂。相比第一代和第二代EGFR-TKI,第三代EGFR靶向治疗药物奥希替尼对导致第一代EGFR-TKI药物失效的T790M突变依然有效,同时疗效方面存在明显优势。
2017年3月24日,奥希替尼在中国正式批准用于既往经EGFR-TKI治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR T790M突变阳性的局部晚期或转移性NSCLC成人患者的治疗,创下了进口药进入中国的最快速度记录。此次奥希替尼在中国获批一线疗法适应证,从递交申请到正式获批历时仅历时10个月,与其在美国获批一线疗法仅隔16个月。
奥希替尼获批一线治疗EGFR突变晚期NSCLC适应证主要是基于III期FLAURA研究的优异结果。
入组人群:共纳入556例未经治疗的局部晚期或转移性EGFR阳性NSCLC患者。
主要研究终点:无进展生存期(PFS)。
次要研究终点:包括总生存期(OS)、客观缓解率(ORR)、疾病缓解时间(DoR)、疾病控制率(DCR)、安全性和生活质量评分(HRQoL)。
治疗方案:随机给予奥希替尼[80 mg,口服(PO)每日1次(QD)]或标准治疗(厄洛替尼150 mg,PO QD或吉非替尼250 mg,PO QD。
研究结果:
➤PFS:奥希替尼组中位PFS高达18.9个月,对照组为10.2个月,疾病进展和死亡风险降低54%,并且在具有脑转移的患者中,奥希替尼组的中位PFS明显优于对照组,奥希替尼组为 15.2个月,对照组为9.6个月。
➤OS:与第一代EGFR TKI相比,奥希替尼显著改善了EGFR突变患者的OS,具体数据将于今年ESMO大会上公布,我们敬请期待!
➤DoR:奥希替尼组中位DoR为17.2个月,对照组为8.5个月。
➤安全性方面:3级以上不良反应发生率,奥希替尼组为33.7%,对照组为44.8%,奥希替尼安全性更好,毒副作用更少。
基于这些结果,奥希替尼已成为EGFR敏感突变患者的优选治疗方案,NCCN指南推荐奥希替尼为EGFR敏感突变患者的首选EGFR TKI。此次在我国获批一线治疗,能让更多EGFR突变NSCLC患者获益,活得更长。


 宫颈癌1b1期是早期吗2026-01-16
宫颈癌1b1期是早期吗2026-01-16 早期胃癌会有头晕吗2026-01-16
早期胃癌会有头晕吗2026-01-16 肝癌晚期吃中药能好吗2026-01-16
肝癌晚期吃中药能好吗2026-01-16 胃癌食管癌会传染吗2026-01-16
胃癌食管癌会传染吗2026-01-16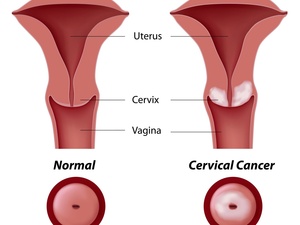 宫颈癌ibl期会死吗2026-01-16
宫颈癌ibl期会死吗2026-01-16 半夜咬牙磨牙是什么症状2026-01-16
半夜咬牙磨牙是什么症状2026-01-16 五味沙棘散调理脾胃吗2026-01-16
五味沙棘散调理脾胃吗2026-01-16 天冷手脚冰凉的原因2026-01-16
天冷手脚冰凉的原因2026-01-16 生姜泡枸杞可以祛湿气吗2026-01-14
生姜泡枸杞可以祛湿气吗2026-01-14 按什么穴位祛体内湿气2026-01-14
按什么穴位祛体内湿气2026-01-14
