作者丨Chemo
来源丨医学界肿瘤频道
9月下旬,CSCO年会于厦门国际会议中心盛大召开。在肺癌免疫治疗专场中,来自中国医学科学院肿瘤医院的王洁教授分享了专题:如何提高免疫检查点抑制剂二线治疗的疗效。随着纳武利尤单抗获批用于EGFR/ALK阴性的晚期或转移性非小细胞肺癌(NSCLC)二线治疗,这一专题解读似乎来得十分应景。
十多年来,随着靶向治疗及其他治疗手段的进步,NSCLC的总体生存状况得到了一定提升。美国SEER数据库最新数据显示[1],NSCLC总体5年生存率达到了18.6%,但对于发生远处转移的晚期NSCLC患者,5年生存率仍然仅有4.7%。
而免疫治疗出现后,这一局面被打破,晚期NSCLC的5年生存率首次提高到了16%[2],相比4.7%翻了近三倍。不同于直接杀伤肿瘤细胞的传统肿瘤治疗手段,免疫检查点抑制剂是利用机体自身的免疫系统杀伤肿瘤。
一方面,抗肿瘤免疫应答通过持续识别和记忆肿瘤抗原,随时间不短增强和扩大。
另一方面,随着免疫应答的扩大,一些细胞毒性T细胞分化为成熟记忆T细胞。即使在原始抗原刺激不存在时,这些细胞依然能够提供长期免疫记忆保护。
尽管免疫治疗相比传统疗法,显著改善了患者的总生存状况,但仍然有一个问题不可回避,即免疫检查点抑制剂单药总体响应率偏低。

图1
从上面这张图我们看到,除了Keynote 024研究中,帕博利珠单抗在PD-L1表达率≥50%的NSCLC患者中,客观缓解率(ORR)达到了44.8%,其余研究中,免疫检查点抑制剂的ORR几乎都徘徊在20%以下。
那么,该如何提高免疫检查点抑制剂二线治疗的疗效呢?
一
利用生物标记物精准识别获益人群
免疫治疗中生物标记物(biomarker)的概念,尽管被提出不过两三年,但已经渐渐为大家所熟知,包括PD-L1、TMB、CD8+ T细胞密度、TCR序列分析等,但需要指出的是,任何单一的生物标记物用于指导免疫治疗均具有局限性,“多重”生物标记物是未来的发展方向。
PD-L1
PD-L1的表达是最为大家熟知的免疫治疗biomarker之一,下面这张表回顾性地总结了CheckMate 017[3]、CheckMate 057[3]、Keynote 010[4]、OAK[5]研究中,PD-1/PD-L1单抗二线治疗晚期NSCLC基于PD-L1表达的总生存(OS)数据。
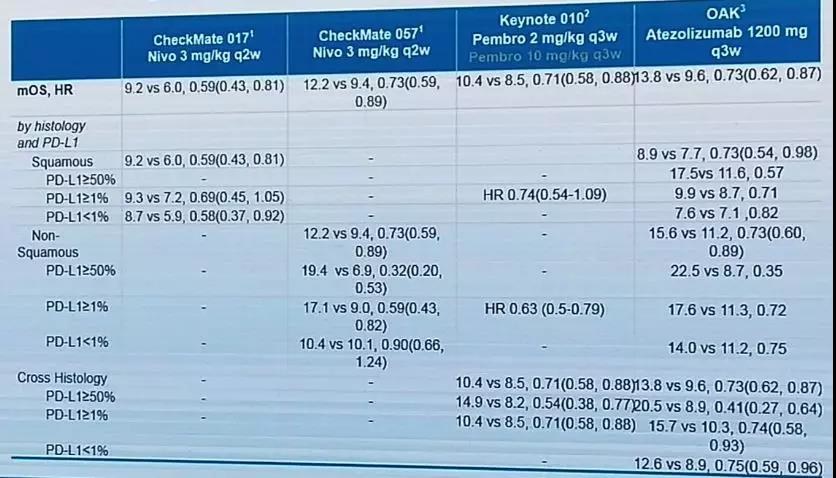
图2
可以发现,在非鳞状NSCLC中,PD-L1表达率越高,患者OS获益越显著;而在鳞状NSCLC中,PD-L1表达率似乎对患者OS获益指导意义不强,仍需要寻找新的biomarker。
肿瘤突变负荷(TMB)
TMB是另一个广受关注的biomarker。下图中,2015年发表于Science的研究和2017年发表于NEJM的CheckMate 026研究[6]分别探讨了TMB与免疫治疗疗效之间的关系。

图3
从无进展生存(PFS)曲线走势可以看出,TMB与免疫抑制剂单药二线疗效在NSCLC中存在显著相关性。相比低TMB(﹤10 Mutations/Mb)的患者,高TMB(≥10 Mutations/Mb)的患者接受免疫检查点抑制剂单药治疗中位PFS显著延长。

图4
同样在免疫联合化疗中,高TMB(≥10 Mutations/Mb)的患者获益也更显著[7]。1年PFS率显著高于低TMB患者。
然而又一个问题出现了,并非所有的患者都能够进行TMB检测。在CheckMate 026研究中,有42%的标本不符合TMB检测要求。我们知道,晚期肺癌中常规的免疫组化、EGFR、ALK的检测都需要肿瘤组织,而TMB检测对肿瘤组织的获取量和质量要求都比较高,尤其在二线、三线治疗,重复活检变得更加困难。
随着技术的进步,除了组织标志物,血液标志物、影像标志物也逐渐得到发展,血液和影像标志物均无创、样本易获得、且可以动态监测。

图5
分析血液TMB(bTMB)和组织TMB(tTMB)的一致性发现[8],在TMB≥30的组织和血液样本中,有1/3的变异信息只来自于血液,1/4的变异信息只来源于组织,剩下的同时来自于血液和组织。也就是说,bTMB与tTMB具有较好的一致性。
但需要知道的是,bTMB仍存在一定的局限性,并不总是能够预测免疫治疗的疗效,研究显示,bTMB对阿特珠单抗的OS预测几乎没有作用[8]。且关于bTMB检测,仍有很多问题需要解答:
到底需要多大的panel:基因数/Panel Size的优化?
选择纳入哪些基因:基因的选择对计算TMB有影响吗?
哪些变异形式应该纳入:算法的优化,例如同义突变及indel?
应该进行基于panel的bTMB与基于WES组织TMB对比。
需要在ICB治疗组中进行bTMB预测价值的分析。
二
火眼金睛,早期识别假性进展、超进展
假性进展的鉴别
假性进展是免疫治疗的一项独特反应模式,表现为肿瘤负荷增大,但患者可以获益从而达到客观缓解或疾病稳定。出现假性进展原因主要有:当淋巴细胞浸润肿瘤时,肿块可能表现为增大或新病灶出现;另外达到适应性免疫反应需要一定时间,假性进展可能表现为肿瘤持续增长直至达到一定程度的缓解。
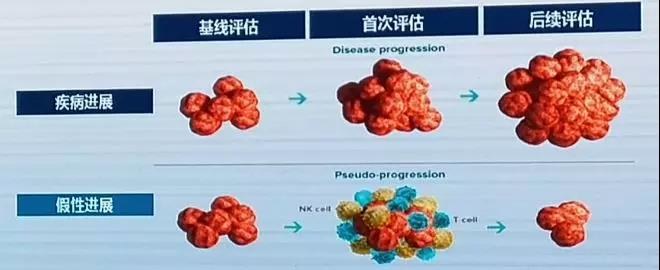
图6
所以对于免疫治疗中,出现肿瘤增大的患者,不要急着停药,需先评估患者的系统症状和PS评分,如果患者症状稳定或改善,提示可能为假性进展。
此外,假性进展的鉴别可以借助ctDNA动态监测。如果ctDNA含量表现为随治疗下降,则可能为假性进展。

图7
如上图,今年发表于JAMA Oncology的这项研究中[9],共125例转移性黑色素瘤患者接受了PD-1单抗治疗,其中29例患者观察到疾病进展(PD),对29例患者进行ctDNA分析(从基线开始到治疗12周的动态变化)发现,20例患者为PD,9例患者为假性进展。
另外,血清IL-8的动态监测也可辅助鉴别假性进展。血清IL-8下降提示假性进展,血清IL-8升高则更倾向于真性进展[10]。
超进展
超进展(HPD)也是免疫治疗中比较特殊的表现。目前HPD还没有比较公认的定义,一些研究认为:根据RECIST标准,与基线相比,治疗期间首次评估疗效时肿瘤生长速率≥基线的两倍的增加为HPD。
HPD并不是免疫治疗特有,在crizotinib、sorafenib、及vemurafenib等TKI治疗后,也观察到超速进展。

图8
目前的研究发现,HPD与年龄存在显著相关性,19%的HPD患者年龄≥65岁。HPD与肿瘤负荷、治疗线数无相关性,PD-1抑制剂和PD-L1抑制剂在HPD上无明显差异。另外有研究观察到,出现HPD的患者多存在MDM2基因扩增。
基于以上证据,我们可以在免疫治疗过程中通过监测基因突变、关注HPD高风险人群,从而做到未雨绸缪,防止HPD突发状况。
三
探寻合适的治疗时间
关于免疫治疗的持续时间,目前的研究表明,1年的疗效不如2年。
CA209-003和KeyNote-010研究表明:PD-1抑制剂治疗2年后停药,大部分患者仍在持续应答。免疫治疗的治疗时间是2年还是持续治疗,目前尚没有定论。
四
进一步探索联合策略
目前,免疫治疗二线都是单药,对于PS评分较好的患者,或许可以考虑联合治疗。
另外对于驱动基因阳性、一线靶向治疗后耐药的患者,以及突变负荷高、突变混乱,没有较好靶向治疗对策的患者,也可能是免疫治疗的合适人群。
总结
目前仍有约60%的NSCLC患者治疗手段非常有限,生存预后不理想;
多种PD-1/PD-L1抑制剂已经成为新二线NSCLC治疗标准;
未来通过biomarker的研究精准识别获益人群以促进二线免疫治疗的疗效;
精细化的分层基础上的合理的联合策略是未来的探索方向。
参考文献
[1] Surveillance, Epidemiology, and End Results Program (SEER) stat Fact Sheets: Lung and Bronchus cancer. Available at: http://seer.cancer.gov/statfacts/html/lungb.html.Accessed June, 2018
[2] Scott Gettinger, et al. J Clin Oncol. 2018; Mar 23:JCO2017770412.
[3] Leora Horn, er al. J Clin Oncol. 2017;35:3924-3933.
[4] Roy S Herbst, et al. Lancet 2016;387: 1540-50.
[5] Rittmeyer A, et al. Lancet 2017;389:255-265.
[6] N Engl J Med. 2017 Jun 22;376(25):2415-2426.
[7] N Engl J Med. 2018 May 31;378(22):2093-2104.
[8] Nat Med. 2018 Aug 6. doi: 10.1038/s41591-018-0134-3.
[9] JAMA Oncol. 2018 Feb 8:el175332.
[10] Ann Oncol. 2017 Aug 1;28(8):1988-1995.


 胃癌恶性肿瘤是癌症吗2026-02-10
胃癌恶性肿瘤是癌症吗2026-02-10 早期胃癌无需化疗吗2026-02-10
早期胃癌无需化疗吗2026-02-10 靶向治疗肿瘤会消失吗2026-02-10
靶向治疗肿瘤会消失吗2026-02-10 宫颈癌还可以怀孕吗2026-02-10
宫颈癌还可以怀孕吗2026-02-10 b超能检查出来宫颈癌吗2026-02-10
b超能检查出来宫颈癌吗2026-02-10 艾滋病手脚冰凉怎么治2026-02-07
艾滋病手脚冰凉怎么治2026-02-07 跪坐能否改善手脚冰凉2026-01-29
跪坐能否改善手脚冰凉2026-01-29 孕妇生了孩子手脚冰凉2026-01-29
孕妇生了孩子手脚冰凉2026-01-29 脾胃失常不胖怎么调理2026-01-29
脾胃失常不胖怎么调理2026-01-29 怎么治疗夜间惊恐发作2026-01-29
怎么治疗夜间惊恐发作2026-01-29
