拜耳公司今天宣布,关键性III期临床研究OASIS 1和2取得积极顶线结果,该研究旨在评估在研产品Elinzanetant与安慰剂相比的疗效和安全性。两项临床研究成功达到全部四个主要终点,与安慰剂相比,治疗组受试者从基线到第4周和第12周,中度至重度血管舒缩症状(VMS,也称为潮热)的频率和严重程度降低在统计学上达到显著性。
两项研究还达到了三个关键次要终点,与安慰剂相比,治疗组受试者从基线到第1周,VMS的频率降低在统计学上具有显著性,睡眠障碍和绝经相关生活质量改善在统计学上也同样具有显著性。在 OASIS 1 和 2 研究中观察到的安全性特征与之前发表的数据总体一致1,2。
“我们对elinzanetant这两项关键III期临床研究的积极结果感到振奋,这增强了elinzanetant作为绝经期管理中非激素治疗选择的潜力” 拜耳处方药事业部执行委员会成员兼全球研发负责人Christian Rommel表示:“我们要感谢参与OASIS研究的女性受试者、她们的家人、所有研究人员以及她们的临床和护理人员,感谢她们为推进绝经期研究付出的时间和承诺。”
Elinzanetant是首个双神经激肽-1,3(NK-1,3)受体拮抗剂,处于临床开发后期阶段,用于与绝经相关的中度至重度VMS的非激素治疗,每日口服一次。
“潮热和睡眠障碍等绝经期症状可带来严重危害,并广泛影响健康和生活质量,但许多女性仍在默默应对,且未得到治疗。” UVA Health教授、中年健康部主任JoAnn Pinkerton博士说:“重要的是,我们在持续开展研究,寻求女性未满足需求的解决方案,我期待公布全部结果。”
OASIS 1 和 2(NCT05042362 和 NCT05099159)是 OASIS 临床开发项目中最先获得结果的 两项III 期研究,详细结果将在即将举行的学术会议上公布。第三项III期研究OASIS 3(NCT05030584)的结果预计将在未来几个月内公布。拜耳计划向药品监管机构提交OASIS 1、2和3研究的数据,申请治疗绝经相关中度至重度VMS的上市许可。





 万万没想到,“神药”二甲双胍会在这“小病”遇滑铁卢?2021-11-09
万万没想到,“神药”二甲双胍会在这“小病”遇滑铁卢?2021-11-09 这4类药,儿童不宜服用!记下来千万别中招2021-10-14
这4类药,儿童不宜服用!记下来千万别中招2021-10-14 国庆小长假想放飞自我?这5个用药规则千万别忘记!2021-09-30
国庆小长假想放飞自我?这5个用药规则千万别忘记!2021-09-30 疾病负担日益加重 新药研发失败率高 AD如何与寿命“赛跑”?2021-09-24
疾病负担日益加重 新药研发失败率高 AD如何与寿命“赛跑”?2021-09-24 长期服用阿片类药物患者换为丁丙诺啡,风险有多大?2021-09-10
长期服用阿片类药物患者换为丁丙诺啡,风险有多大?2021-09-10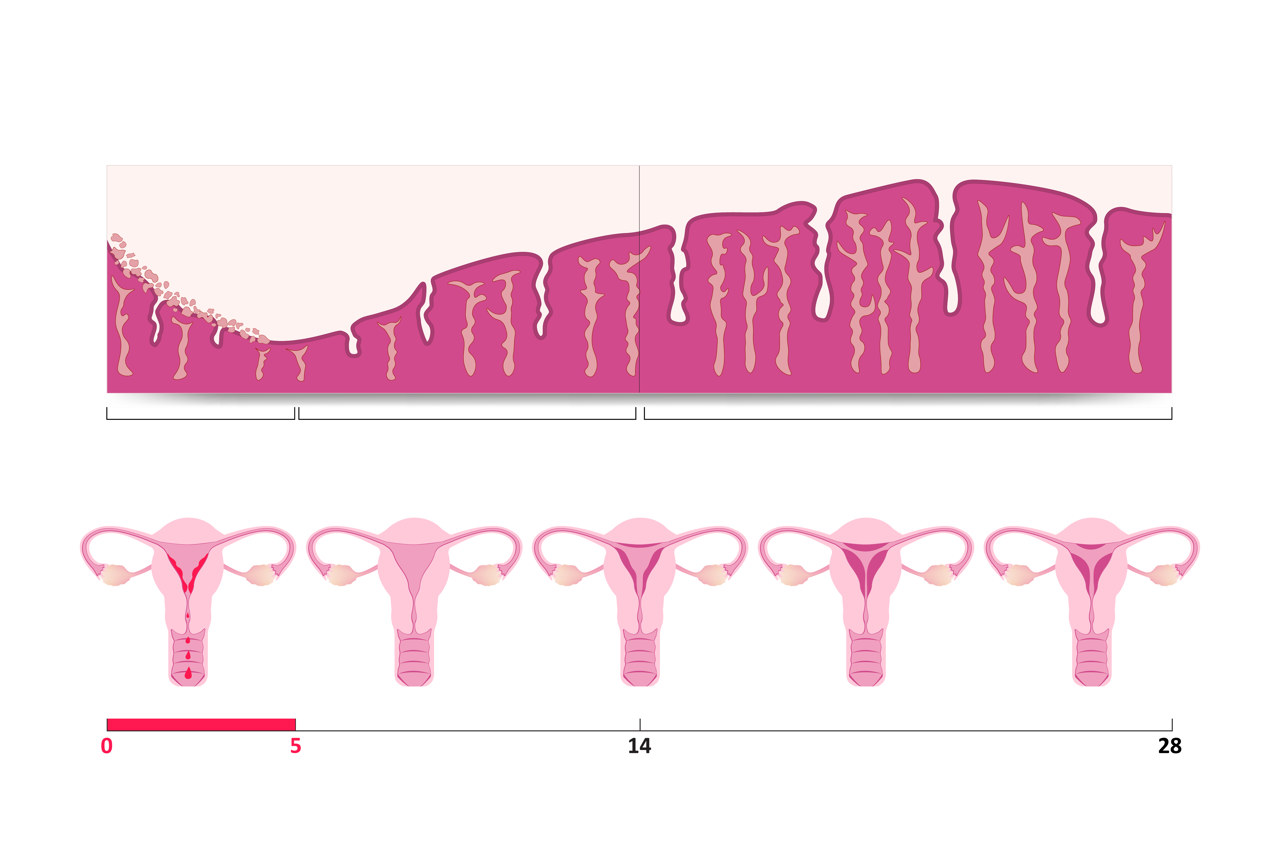 排卵期白带的变化2025-07-13
排卵期白带的变化2025-07-13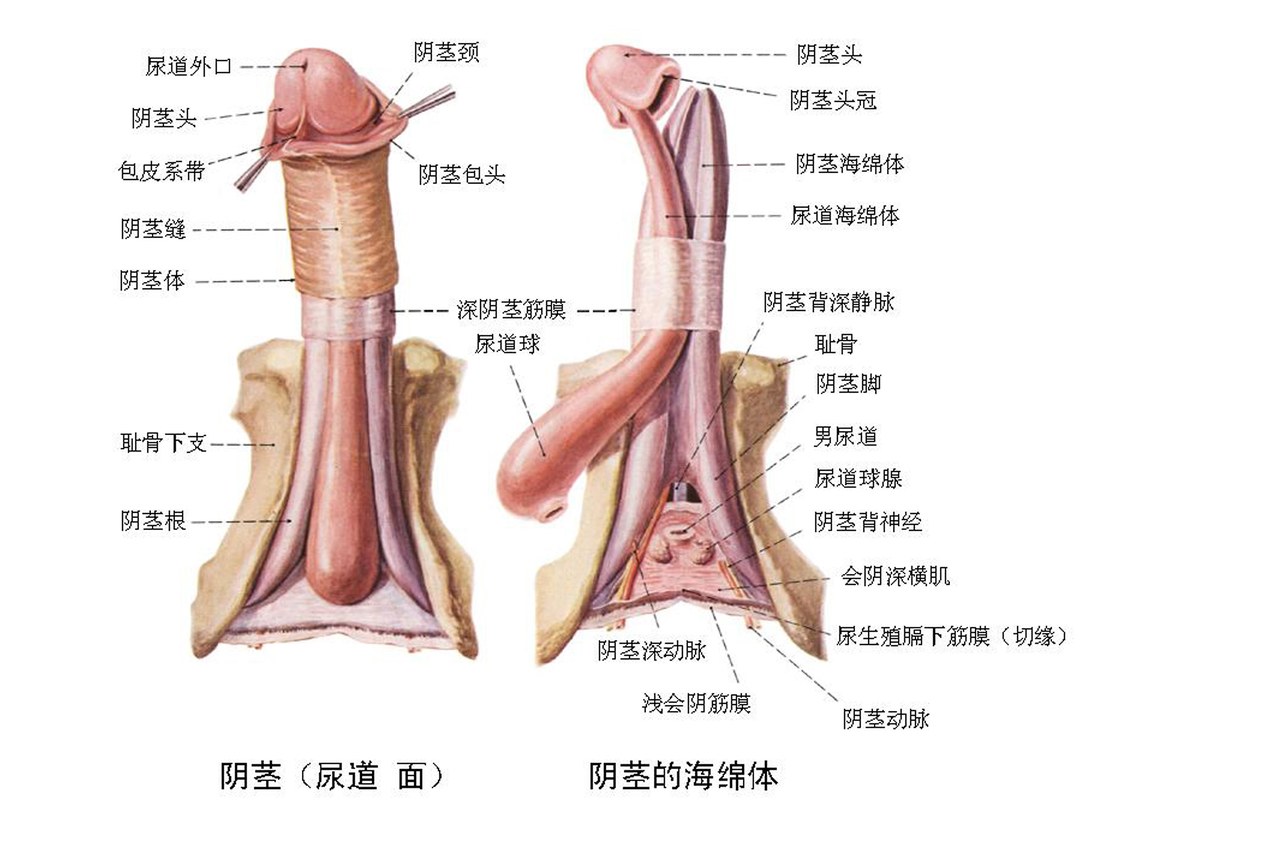 阴道口大小和什么有关2025-07-13
阴道口大小和什么有关2025-07-13 18岁之后性需求会越来越强烈吗 人的性欲是如何变化的2025-07-13
18岁之后性需求会越来越强烈吗 人的性欲是如何变化的2025-07-13 房事射精过快,早泄2025-07-13
房事射精过快,早泄2025-07-13 生力片在同房前多久吃,效果最好2025-07-13
生力片在同房前多久吃,效果最好2025-07-13
