近年来,抗生素、消毒剂的不恰当使用导致金黄色葡萄球菌的耐药菌株大幅度增加,甚至还出现了多重耐药菌的情况。
今天就由山东省立医院呼吸科张嵩老师给我们详细讲解一下金黄色葡萄球菌为何总是耐药。

1 金黄色葡萄球菌 VS β-内酰胺类抗生素
多数医院获得性金黄色葡萄球菌肺炎(HA-MRSA)对甲氧西林和所有β-内酰胺类耐药,且常为多重耐药,可选择药物十分有限。
而社区获得性金黄色葡萄球菌肺炎(CA-MRSA)通常仅对β-内酰胺类耐药,对非β-内酰胺类抗生素敏感。
金黄色葡萄球菌对β-内酰胺类耐药性与青霉素结合蛋白(PBPs)有关。
PBPs是广泛存在于细菌表面的一种膜蛋白,是合成金黄色葡萄球菌的重要蛋白酶系统,也是β-内酞胺类抗生素的主要靶位。当环境药物浓度达到最低抑菌浓度时,β-内酰胺类抗生素会与PBPs上的靶点结合,使其乙酰化,致使转肽酶TPase丧失活性,导致细菌细胞壁无法形成从而杀死敏感菌。
金黄色葡萄球菌产生了一种独特的PBP,称为PBP2a。β-内酰胺类抗生素很难与PBP2a上的靶点结,所以PBP2a的存在能使细菌的细胞壁继续合成,从而使金黄色葡萄球菌表现出耐药性。
不仅如此,调节PBP2a染色体的甲氧西林耐药基因(mecA)其所在的DNA片段还能不断获得性积累其他耐药基因,从而使得金黄色葡萄球菌产生多重耐药性。
2 金黄色葡萄球菌 VS 大环内酯类抗生素
金黄色葡萄球菌对大环内酯类抗生素的耐药性主要由3个机制产生。最重要的一个机制是由erm基因编码产生的核糖体甲基化酶对抗生素结合位点进行修饰后,导致核糖体对大环内酯类抗生素的亲和力下降,第二是外排泵将抗生素主动排出菌体外,第三个是合成大环内酯类抗生素失活酶。
大环内酯类抗生素不仅对金黄色葡萄球菌耐药,对链球菌、支原体也同样耐药,所以基本上不选择这类抗生素,不仅如此,大环内酯类抗生素还会诱导克林霉素耐药,所以用药选择上也尽量避免选择克林霉素。
3 金黄色葡萄球菌 VS 氟喹诺酮类药物
氟喹诺酮类药物杀菌主要通过抑制细菌DNA靶位酶,阻断细菌遗传物质复制与转录,从而使细菌死亡。
金黄色葡萄球菌对氟喹诺酮类的耐药主要与药物作用靶位酶的改变和药物在菌体内蓄积量减少有关。
一方面,由于金黄色葡萄球菌靶酶基因位点突变影响氟喹诺酮类药物与靶酶的结合,从而避免了细菌的死亡;
另一方面,金黄色葡萄球菌对氟喹诺酮类外排增加和摄入减少,尤其是外排增加导致氟喹诺酮类在体内积蓄量减少,从而不能发挥抗菌作用。
4 金黄色葡萄球菌 VS 氨基糖苷类药物
金黄色葡萄球菌对氨基糖苷类药物耐药的主要机制是细菌获得氨基糖苷类修饰酶基因,使药物与核糖体的结合不紧密而不能发挥抗菌作用。
5 金黄色葡萄球菌 VS 糖肽类药物
万古霉素等糖肽类药物的耐药机制主要包括细菌壁增厚、肽聚糖交联减少、青霉素结合蛋白的改变、抗生素诱导、调节基因改变、耐药基因转移、酶活性降低等。
存在于金黄色葡萄球菌细胞壁肽聚糖层上的D-丙氨酰酸残基与万古霉素的结合可将大部分的药物阻于细胞壁外,降低对细菌的杀伤力。
另外肽聚糖单体异常增加,由此可结合更多的万古霉素,使药物不能与细菌的靶位接触不能发挥抗菌作用。
作用于细胞壁的糖肽类药物使细胞壁增厚,降低药物对细菌的杀伤。
抗生素的诱导也是细菌耐药的一个重要因素,金黄色葡萄球菌耐药菌株中的耐药基因可以从肠球菌的质粒中转移,因此耐药基因的转移也是细菌产生耐药的一个重要原因。
而微管系统的存在以及与万古霉素有协同作用的水解酶、溶解酶等酶性降低等也是细菌耐药的一个不可忽视的方面。
6 金黄色葡萄球菌 VS 恶唑烷酮类药物
恶唑烷酮类药物如利奈唑胺的耐药机制包括核糖体突变、核糖体蛋白突变以及耐药基因产生。
此外,耐药基因通过影响核糖体干扰了抗生素定位以及与细菌的结合进而影响抗菌活性,可介导恶唑烷酮类(如利奈唑胺)、苯丙醇类(如氟苯尼考)、林克酰胺类(如克林霉素)、截侧短耳素(如泰妙菌素)、链阳菌素A(如奎奴普丁、达福普汀)5类药物耐药。因此,携带耐药基因也是金黄色葡萄球菌耐药的重要原因。



 刘泽群
刘泽群
 吴泽霖
吴泽霖
 何峰
何峰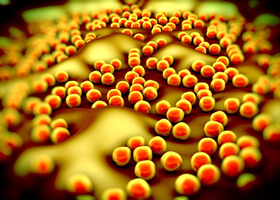
 杜虹瑶
杜虹瑶
 郭兮恒
郭兮恒
 周博
周博
 刘芳
刘芳 万万没想到,“神药”二甲双胍会在这“小病”遇滑铁卢?2021-11-09
万万没想到,“神药”二甲双胍会在这“小病”遇滑铁卢?2021-11-09 这4类药,儿童不宜服用!记下来千万别中招2021-10-14
这4类药,儿童不宜服用!记下来千万别中招2021-10-14 国庆小长假想放飞自我?这5个用药规则千万别忘记!2021-09-30
国庆小长假想放飞自我?这5个用药规则千万别忘记!2021-09-30 疾病负担日益加重 新药研发失败率高 AD如何与寿命“赛跑”?2021-09-24
疾病负担日益加重 新药研发失败率高 AD如何与寿命“赛跑”?2021-09-24 长期服用阿片类药物患者换为丁丙诺啡,风险有多大?2021-09-10
长期服用阿片类药物患者换为丁丙诺啡,风险有多大?2021-09-10 长期磨牙的危害2025-08-06
长期磨牙的危害2025-08-06 吕梁甲状腺功能亢进去哪里治权威2025-08-06
吕梁甲状腺功能亢进去哪里治权威2025-08-06 雅安椎间盘突出去哪里治好2025-08-06
雅安椎间盘突出去哪里治好2025-08-06 攀枝花治疗乳腺增生权威医院推荐2025-08-06
攀枝花治疗乳腺增生权威医院推荐2025-08-06 济宁治疗多发性硬化医院推荐2025-08-06
济宁治疗多发性硬化医院推荐2025-08-06
